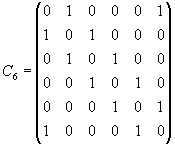
Конструктивная математика
Акимов О.Е.
33. Матрицы смежности и линейчатые спектры
Робертс [59], во многом опираясь на идеи Хюккеля, изложил метод молекулярных орбит для расчета энергетического спектра молекул углеводородов. Он не касается прямого и обратного пространства кристалла, а дает лишь представление о значениях энергии. Идея этого метода основывается на модели сильной связи, напоминающую рассмотренную выше, в которой, однако, можно проводить вычисления спектра. Им были найдены и подробно проанализированы энергетические уровни и волновые функции молекулы бутадиена
CH2 = CH – CH = CH2.
Авторы работы [60] считают, что разупорядоченная решетка аморфного полупроводника имеет кластерную структуру, т.е. некоторые группы атомов могут быть представлены автономной устойчивой системой, как если бы они образовывали отдельную молекулу. Кластерная модель для расчета энергетического спектра разупорядоченного полупроводника использовалась многими исследователями. Обзор этих моделей можно найти в работе Харрисона [49].
Чинг, Чун и Хубер в 1976 г. опубликовали работу, где представили результаты расчета энергетического спектра аморфного кремния (a-Si). Кластеры, состоящие из 20 – 40 атомов a-Si дают достаточное количество энергетических полос, чтобы можно было ориентироваться на реальную плотность состояний. Далее, варьируя по величине отклонения от строгой тетраэдрической структуры, можно добиться количественного согласия экспериментальной плотности уровней в a-Si с пропорциональным числом вычисленных линий, приходящихся на ту или иную область энергии. Варьирование осуществлялось по четырем длинам связи: 0.934, 1.019, 1.037, 1.036 (длина связи в кристаллическом кремнии принята за 1,000) и шести углам: 95.3°, 131.3°, 132.0°, 129.0°, 79.8°, 88.5°.
Суть данной модели сильной связи заключается в матрице смежности, которая несет информацию о геометрической конфигурации молекулярного или кластерного соединения атомов вещества. Пусть даны четыре одинаковых атома, которые расположены в вершинах тетраэдра. Энергетическое состояние электронной системы каждого атома одинаковое; обозначим его через а. Взаимодействие между всеми атомами, в силу симметрии, также одинаковое; обозначим обменное взаимодействие через b. Составим матрицу смежности графа-тетраэдра, который является главным элементом алмазоподобных полупроводников, и отыщим ее собственные значения:
=
=
= x4 – 6x2 + 8x – 3 = (x +3) (x – 3)3 = 0;
x = (a – E)/b, E1 = a + 3b, E2,3,4 = a – b.
Однократно вырожденное состояние E1 ассоциируется в s-состоянием, а трехкратно вырожденное E2, 3, 4 — с p-состоянием. В a-Si тетраэдры искажены, поэтому вырождение снимается. Так как в тетраэдрический кластер входят по одной связи от четырех различных атомов, то четыре энергетических уровня приравниваются к спектру одного атома. Энергетические уровни от кластеров из 2 – 3 атомов довольно сильно зависят от принятой конфигурационной схемы кластера. В a-Si каждый атом соединен с четырьмя соседними. Следовательно, за основу может быть выбран иной тетраэдр с матрицей смежности следующего вида:
= x3(x2 – 4) = 0;
E1,2,3 = a, E4,5 = a ± 2b.
В этом случае также можно говорить о трехкратном p-состоянии и двух (связывающем и разрыхляющем) s-состояниях. Энергетическая щель между этими энергиями, в отличие от предыдущего варианта, равна 2b. Чем больше атомов в кластере, тем меньше чувствительность энергетического спектра к конкретному виду матрицы.
Чинг, Чун и Хубер рассчитали энергетические уровни четырех кластеров, состоящих из 1, 5, 17 и 29 атомов (рис. 65). На линейчатых спектрах хорошо видна запрещенная зона. Края валентной зоны и зоны проводимости размыты, как и должно быть, согласно теории разупорядоченных систем [61], [62], [63]. Некоторые состояния попадают в центральную область запрещенной зоны, что также регистрируется в опытах с a-Si.
Рис. 65
Для бутадиена Робертс составил структурную матрицу вида:
= x4 – 3x2 + 1 = 0,
= ±1.618, ±0.618.
Числовой расчет коэффициентов вхождения атомных орбиталей в молекулярные Робертс осуществил по минорам исходной матрицы. В результате подсчетов у него получились следующие линейные комбинации:
ψ1 = 0.3717χ1 + 0.6015χ2 + 0.6015χ3 + 0.3717χ4,
ψ2 = 0.6015χ1 + 0.3717χ2 – 0.3717χ3 – 0.6015χ4,
ψ3 = 0.6015χ1 – 0.3717χ2 – 0.3717χ3 + 0.6015χ4,
ψ4 = 0.3717χ1 – 0.6015χ2 + 0.6015χ3 – 0.3717χ4.
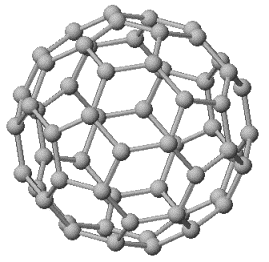
Мы говорили, что углерод имеет четыре аллотропных конфигурации (они показаны на рис. 66): тетраэдрическую (1), гексагональную (2), линейную (3) и сферическую (4). В действительности же их намного больше (рис. 67), поскольку атомы углерода могут образовывать множество промежуточных пространственных структур с меньшим запасом прочности, чем у четырех перечисленных полиморфизмов. Самая устойчивая фуллереновая структура состоит из 60 атомов углерода и обозначается С60. Атомы расположены в вершинах усеченного икосаэдра, который имеет следующие элементы: n = 60, f = 32, m = 90. Из 32 граней 12 пятиугольных и 20 шестиугольных.
(1)
(2)
(3)
4)Рис. 66
(5)
(6)
(7)(8)
(9)(10)
Рис. 67
Самая неустойчивая замкнутая фуллереновая структура С20 (5) образована 12-ю пятиугольными гранями, что дает додекаэдр. Неустойчивость возникает из-за удаленности этой фигуры от сферической формы; ее острые углы вызывают напряжения и, в конце концов, конструкция упруго раскрывается, образуя более устойчивую форму в виде чаши (6) с кольцами симметрии С5 и С6. Получают С20 из молекул С20Н20 (7) путем замещения атомов водорода атомами брома, затем удаляются и атомы брома. Кластеры С20 существуют короткое время, но их присутствие регистрируется масс-спектрографом. Приборы фиксируют также, что наряду с чашами при распаде С20 могут возникать линейчатые кольца (8), устойчивость которых тоже невысока. Вторым по устойчивости образованием является немного вытянутая сфера С70. Сравнительно большая доля (все зависит от технологических условий) подобных кластеров постоянно присутствует в среде из С60. Оказалось также, что углеродные атомы могут образовывать сетчатые изогнутые трубки (9), несмотря на всю сложность их конструкций.
В работе [53] проанализированы линейчатые спектры, получающиеся от фуллереновых структур. Для шести атомов углерода, расположенных в вершинах равностороннего шестиугольника, матрица смежности похожа на матрицу для бутадиена. Поскольку диагональные элементы определяют точку отсчета энергетического спектра, приняв ее в C6 за ноль, мы получаем матрицы смежности как в теории графов.
В табл. 42, в соответствии с симметрией шестиугольника, приведены представления группы D6h, их базисные функции (ψ), собственные значения энергии (E), выраженные в эВ, кратность вырождения (m), а также число электронов (n) на каждом энергетическом уровне. За энергию связи здесь была принята энергия связи атомов углерода в структуре фуллерена С60 ( a = 2.38 эВ ). Разность энергий между уровнем дна ЗП и потолка ЗВ составляет энергию ЗЗ Eg = 4.76 эВ.
Таблица 42
Г(D6h) ψ E m n Г2u 6–½ · (1 – 2 + 3 – 4 + 5 – 6) 4.76 1 0 Г6g 8–½ · (1 – 2 · 2 + 3 + 4 – 2 · 5 + 6)
2–1 · (–1 + 3 – 4 + 6 )2.38 2 0 Г5u 8–½ · (1 – 2 · 2 – 3 + 4 + 2 · 5 + 6)
2–1 · (1 – 3 – 4 + 6)–2.38 2 4 Г1g 6–½ · (1 + 2 + 3 – 4 + 5 + 6 ) –4.76 1 2 Матрица смежности фуллерена С20 составлена по планарному графу, изображенному на рис. 68 и идентична графу додекаэдра. Собственные значения матрицы смежности отождествляются с энергией атомного кластера фуллерена равны:
3,
,
,
, 1, 1, 1, 1, 1, 0,
0, 0, 0, –2, –2, –2, –2, –
, –
, –
.
Рис. 68
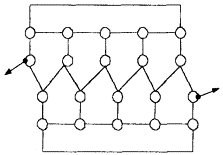
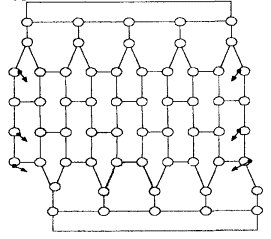
Аналогично составляется матрица смежности для фуллерена С60 по планарному графу, изображенному на рис. 69 (оборванные связи соединяют крайние атомы на этом же ряду).
Рис. 69
Ее собственные значения равны:
E1 = –1, E2 = 2, E3 = –3,
,
,
,
,
,
.
В табл. 43, согласно симметрии икосаэдра, приведены представления группы Yh, собственные значения энергии с E1 по E15, их значения, выраженные в эВ, кратность вырождения (m) и число электронов на уровнях (n). Ширина ЗЗ для С60 равна Eg = 0.757a = 1.8 эВ.
Таблица 43
Г(Yh) Ei E m n Г3 E1 6.24 3 0 Г4 E2 6.09 4 0 Г4 E3 4.76 4 0 Г5 E4 3.85 5 0 Г2 E5 3.42 3 0 Г5 E6 3.10 5 0 Г2g E7 0.91 3 0 Г2u E8 0.33 3 0 Г5u E9 –1.47 5 10 Г4g Г5g E10 –2.38 9 18 Г4 E11 –3.71 4 8 Г3 E12 –4.33 3 6 Г5 E13 –5.47 5 10 Г3 E14 –6.56 3 6 Г1g E15 –7.14 1 2 Сфероид фуллерена С70 получается из сферы С60, если в его граф (рис. 69) включить еще один горизонтальный ряд из 10 атомов. За счет этого элемента разупорядочения группа икосаэдра Yh теряет многие элементы своей симметрии, в частности, из шести осей пятого порядка остается одна. Это приводит к расщеплению трех-, четырех- и пятикратно вырожденных линий спектра С60.
Подобная перестройка базовой конструкции С60 дает ключ к пониманию образования трубчатой структуры, которая изображена на рис. 66 (10). Она получается путем включения в граф С70 дополнительных колец из 10 атомов. Промежуточные формы С80 и т.д. существуют недолго, но длинные цилиндры с открытыми торцами является, видимо, долгоживущей конструкцией.
На рис. 70, взятом из работы [53], дается сравнение линейчатых спектров С60 (слева) и С70 (справа).
Рис. 70
Представление группы симметрии С70 можно получить по группе симметрии икосаэдра Yh (индекс h указывает на наличие центра инверсии), если икосаэдр рассечь пополам горизонтальной плоскостью и в точках сечения десяти ребер установить вершины. Напомним также, что группа икосаэдра и додекаэдра (целых или усеченных) одна и та же, подобно тому, как симметрия куба, в силу двойственности, описывается группой октаэдра Oh. Собственные векторы можно восстановить по таблице характеров, матрице смежности С60 и собственным значениям E1 – E15.
Аналогичным образом можно построить граф С80, составить по нему матрицу смежности, найти ее собственные значения и попытаться ответить на вопрос, почему данная система обладает низкой устойчивостью. Граф фуллереновой трубки представляет собой «коврик», часть которого образована четырьмя средними рядами графа С60, где может быть 5, 10, 20 узлов в ряду, как это показано на рис. 69. Его симметрия определяется симметрией диэдра с осью 5-го порядка.
Подобная методика построения и изучения устойчивых систем атомов имеет прямое отношение к исследованиям Майера и Томсона, проведенным еще в начале XX в. на модели из магнитных иголок, установленных на плавающих плотиках (см. п.22 Модель атома Томсона). Выбор модели атома Томсон осуществил верно: в основе ее лежит понятие об устойчивости системы, т.е. стационарный принцип. Динамическая модель атома, подобно Солнечной системы (см. п. 21 Модель атома Бора), не имеет математической перспективы. Более того, сама модель Солнечной системы, как показывают синхронизмы, может описываться в дискретных понятиях (см. п. 35. Дискретная гравитация и аттракторы). Томсон не пользовался методами дискретной математики; его математический аппарат был слишком громоздким и непонятным для большинства молодых физиков, которые не владели математикой в его объеме, а потому восприняли динамическую модель, вероятностную интерпретацию волновой функции и копенгагенскую философию формально-феноменологического характера.
Несколько слов о связи атомов углерода. Алмаз прозрачен, графит имеет черный цвет, карбин — белое вещество с промежуточной плотностью между алмазом и графитом, фуллерен С60 — желто-коричневого цвета, С70 — красно-коричневого цвета. Цветность как раз во многом и определяется природой химической связи. В фуллерене к каждой вершине усеченного икосаэдра подходит две одинарных и одна двойная связь (одинарные чуть длиннее двойной). Поскольку фуллерен — наследник графитовых гексагональных слоев, его организация напоминает графит с гибридными связями типа σπ2. В алмазе длина σ-связи 1.54 Å, в графите между атомами в слое расстояние 1.42 Å и 3.35 Å между слоями. В фуллерене длина ребра, соединяющего две шестиугольные грани, равна 1.432 Å, ребро, соединяющее две пятиугольные грани, равно 1.388 Å (для сравнения: непредельная двойная π-связь в карбине равна 1.34 Å); радиус фуллереновой сферы равен 3.512 Å, т.е. чуть больше расстояния между слоями графита. Сетчатая оболочка фуллерена очень прочна; внутри сферы может удерживаться тяжелый атом металла: K, Na, Cs, Sr … и даже уран. В нагретом состоянии сфера быстро вращается. При определенных условиях фуллерен проявляет сверхпроводящие свойства, что также продиктовано природой химической связи между атомами углерода.
По фуллерену имеется большая и разнообразная литература. История его открытия обычно начинается с упоминания о работах Крето и Смолли, которые в 1985 г., исходя из идеи симметрии многоатомных кластеров углерода, предложили форму усеченного икосаэдра. Задолго до этого была известна также высокая прочность этого архимедова полуправильного многогранника. Из всех возможных сетчатых конструкций, ребра усеченного икосаэдра испытывают наименьшие напряжения, причем равномерно распределенные по всей поверхности. Поэтому эта форма тела и была в 1948 г. принята для футбольного мыча. Название «фуллерен» произошло от фамилии американского архитектора Ричарда Баксминстера Фуллера, который использовал сетчатую конструкцию в строительстве куполов.
В экспериментах Ролфинга, Кэлдора и Кокса по ранее разработанной технологии получения углеродных кластеров путем лазерного испарения графита были обнаружены относительно стабильные образования Cn c индексом n = 20, 24, 28, 32, 40, 44, 50, 58, 60, 70, 72, 78, 80, 82 и т.д. Имеются также достаточно устойчивые конструкции С240 и С540, по-видимому, трубчатого строения. При термической обработке графита в угольном конденсате образуются кластеры только с четным число n. Количественные пропорции между ними меняются в зависимости от температуры. Например, при температуре 600°С имеем N(С60) : N(С70) = 2 : 1, а при температуре 500°С это отношение равно уже 12 : 1.
Фуллереновые образования Cn были обнаружены даже в спектре звезд красных-гигантов. Однако выделить фуллерен в чистом виде долгое время не удавалось. Наконец, в мае 1990 г. Дональд Хуффман (США) и Вольфганг Крэтчмер (Германия) получили С60 в чистом виде, который может храниться длительное время при комнатной температуре. Уже в 1991 г. фирма «Стрем» освоила технологию получения С60 и продавала его для всех желающих по цене 2000 долларов за грамм. Такова краткая история открытия этого перспективного материала.